Rafinarea — purificarea metalelor nobile de impurități și separarea acestora se realizează în rafinăriile noastre centralizate, care dispun de echipamente și condiții pentru a efectua prelucrările necesare cu pierderi reduse.
Rafinăriile primesc aurul schlich și nativ separat prin concentrarea gravitațională a minereurilor și a zăcămintelor, aurul din amalgame, metalul doré din nămolurile rezultate din electroliza cuprului și deșeurile din producția de plumb. De asemenea, reciclează deșeuri industriale și menajere, monede vechi, aliaje obținute din materii prime secundare și alte materiale.
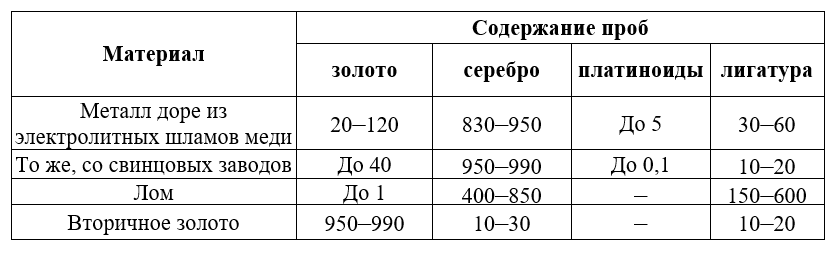
În afară de aur și argint, al căror raport masic variază foarte mult, în materiile prime se găsesc metale platinate, cupru, plumb, antimoniu, fier, staniu, bismut și alte impurități.
Conținutul de metale nobile în aliaje este de obicei exprimat prin probe — miimi de masă, suma impurităților din metalele de bază se numește ligatură. Tabelul 24 oferă informații rotunjite, aproximative privind compoziția principalelor tipuri de materii prime.
Loturile separate de materii prime sunt adesea mici în masă și eterogene, astfel încât pentru calcularea mediei și clarificarea calculelor cu furnizorii se utilizează topirea de acceptare în cuptoare cu inducție și se testează lingourile rezultate.
Pentru a separa ligatura și masa principală de argint, aliajele lichide din aceleași cuptoare în creuzete din grafit sunt suflate cu clor. Toate metalele sunt clorurate, clorurile sunt aprinse, dar ele sunt dizolvate în principal în zgură, pentru formarea primară a căreia se încarcă borax, sodă și nisip. Din următoarele date privind potențialele izobarice de formare a clorurilor la 1200 °C și punctele lor de fierbere putem judeca aproximativ cursul clorurării:

În primul rând, clorurile elementelor ligatură, apoi AgCl și, în sfârșit, AuCl se aprind și trec în zgură.3. La prima apariție a semnelor de clorinare a aurului purjarea este oprită, metalul din eșantionul 995 este turnat în butoaie și predat fondului monetar sau purificat suplimentar prin electroliză, așa cum este descris mai jos. Aceasta din urmă este întotdeauna necesară în cazul conținutului de platinoid.
Zgură clorurată constă în principal din AgCl și CuCl, este zdrobită, încărcată în saci, care sunt apoi introduși într-o baie de acid sulfuric diluat împreună cu foi de fier. Argintul este astfel redus de ionii Fe 2+ :
AgCl + Fe 2+ = Ag + Fe 3+ + Cl,
clorura de cupru este oxidată
CuCl + Fe 3+ = Cu 2+ + Fe 2+ + Cl.
Penetrând prin țesutul sacilor, Cu 2+ sunt cimentați de fier. Ionii Fe 3+ sunt, de asemenea, reduși de fier, astfel încât sunt foarte puțini în soluție și echilibrul reacției de reducere a argintului de către fier este deplasat spre dreapta. Reducerea suficient de completă a argintului se realizează în două zile la o temperatură a soluției de 90-100 °C.
Precipitatul de argint cimentat se presează, se topește și se toarnă în anozi de 10 kg sub formă de plăci cu grosimea de aproximativ 10 mm, care nu trebuie să conțină mai mult de 200 de probe de aur și 75 de probe de ligatură.
Electroliza argintului
Electrolitul este o soluție de AgNO3 cu o activitate de 1 mol/l (până la 100 g/l Ag).
Atunci când anozii se dizolvă, argintul, cuprul, plumbul, bismutul și alte impurități trec în soluție. Aurul cade sub formă de nămol pulverulent care conține metale platinice, seleniu, telur, sulf și alte impurități insolubile în electrolit.
Bazele catodice sunt realizate din foi subțiri de argint sau aluminiu.
Precipitatul catodic de argint are o structură cristalină liberă și grosieră; acesta este ușor de îndepărtat de pe baza catodului și cade pe fundul băii. Pentru a preveni amestecarea precipitatului de argint pur și a nămolului de aur, anozii sunt plasați în saci de pânză.
Anozii cu o grosime de aproximativ 10 mm sunt dizolvați timp de aproximativ o zi, după care reziduul nedizolvat este returnat la topitorie, nămolul aurifer este evacuat din capacele anozilor, iar cristalele de argint pur sunt extrase de pe fundul băii cu ajutorul unor palete de aluminiu holey.
Densitatea curentului nu trebuie să depășească 400-600 A/m 2 , electrolitul trebuie agitat energic și nu trebuie să permită o acumulare semnificativă de impurități, în special cupru, care, pentru a evita contaminarea precipitatului catodic, nu trebuie să fie în soluție mai mult de 4-5 %.
Dacă aurul este mai mare de 200 de probe, acesta pasivează anozii și începe să elibereze oxigen, iar tensiunea pe baie crește în consecință.
Băile cu o capacitate de până la 0,6 m 3 sunt fabricate din plastic vinilic și întărite cu rame din lemn sau fier. Temperatura electrolitului de aproximativ 40 ° C este menținută datorită căldurii generate de curent. Pentru agitare, soluția este agitată cu aer. Tensiunea pe baie în funcție de compoziția electrolitului și de densitatea curentului este de 0,8-2,6 V, iar consumul de energie este de 300-600 kWh/t.
Precipitatul de argint după spălarea cu acid azotic diluat, apă și refolosire are o puritate de 999,9 probe. Pentru clienții individuali, se obțin eșantioane de 999,99 sau 999,999 prin electroliză repetată.
Electrolitul uzat este epuizat cu argint în băi separate cu anozi din aliaje de calitate inferioară.
Electroliza aurului
Electroliza primește metal după clorinare și nămol de la electroliza argintului, supus în prealabil unei purificări chimice în mai multe etape. Toate acestea sunt topite în cuptoare cu inducție și turnate în anozi dreptunghiulari care cântăresc 2-3 kg fiecare. Anozii sunt contaminați cu argint, metale de platină și relativ puțin cu ligatură.
Electrolitul este o soluție de NACCl4 și HCl (până la 200 g/litru de Au și 80 g/litru de HCl). Aurul este dizolvat prin reacții:
Ац + 4Сl — — 3е = АцСІ — 4; E° = 0,93 V,
Ац + 2Сl — — e = АцСІ — — 2; E° = 1,11 V.
Apariția ionilor AuCl — — 2 ionii sunt posibili datorită polarizării concentrației la o densitate mare de curent sau datorită formării unei cruste de AgCl pe anod; cu toate acestea, ei sunt imediat upproporționați odată cu eliberarea precipitatului metalic, căzând în nămol:
AcCl — 2 = AuCl — 4 + 2Au + 2Cl — .
La aciditate și temperatură insuficiente, anozii de aur pasivizează, dizolvarea lor se oprește și începe să se elibereze clor
Oxigenul nu este eliberat din cauza suprasolicitării acestuia asupra aurului.
Electroliza se efectuează la 50-60 °C. Platina și paladiul se dizolvă și se acumulează în electrolit:
Pt + 4Cl — — — 2e = PtCl 2- 4 ; E° = 0,73 V,
Pd + 4Cl — — 2e = PtCl 2- 4; E° = 0,62 V.
Legăturile constitutive: cuprul, plumbul, bismutul, fierul, staniolul, antimoniul și alte metale formează ioni simpli sau cloruri complexe, ele de obicei nu provoacă dificultăți în dizolvarea anodului. Fierul, trecând în soluție sub formă de Fe 2+ , reduce aurul, mărind trecerea acestuia în suspensie:
AcCl — 4 + 3Fe 2+ = Au + 3Fe 3+ + 4Cl — .
Argintul dă o clorură insolubilă.
Dacă în aliaj există mai puțin de 50 de probe de argint, clorura acestuia nu provoacă complicații. La conținuturi mai mari, AgCl acoperă anodul cu o crustă puternică mai mult sau mai puțin densă, împiedicând dizolvarea aurului.
Conform metodei lui Volville reușește să dizolve anozii de aur, care sunt până la 200 de probe de argint, folosind curent asimetric. În acest scop, împreună cu curentul continuu, se trece prin baie un curent alternativ de intensitate aproximativ egală.
Probabilitatea de contaminare a precipitatului catodic cu impurități este scăzută; cu toate acestea, platina și paladiul pot fi depuse împreună cu aurul, în special la densități de curent ridicate. Pentru a evita acest lucru, trebuie evitate concentrațiile de platină de peste 50 g/litru și concentrațiile de paladiu de peste 15 g/litru. Alte impurități dintr-o soluție care conține cel puțin 100 g/litru de aur nu trebuie să fie mai mari de 90 g/litru Cu; 1,5 g/litru Pb; 4 g/litru Te și 2% Fe.
Electrolitul uzat este golit de aur în băi separate cu anozi de grafit, după care aurul rezidual și platinoizii sunt separați din acesta prin diferite metode.
Electroliza aurului se realizează în băi de porțelan, rareori în băi de vinil-plastic cu o capacitate de 25 litri. Anozii, în număr total, de exemplu 15, sunt suspendați pe tije de argint, trei la rând, în dreptul fiecărui rând fiind plasat un catod comun din folie de aur canelată cu grosimea de 0,2 mm. Băile sunt instalate în băi de apă, electrolitul este agitat cu aer.
Densitatea totală a curentului continuu și alternativ atinge 1500 A/m 2 , tensiunea pe baie este de aproximativ 1 V. Puritatea nămolului catodic după curățarea mecanică cu perii și apoi spălarea cu acid clorhidric și amoniac este de 999,9 probe.