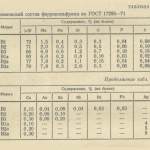
În timpul topirii oțelului într-un cuptor cu arc, oxigenul intră în metal și este parțial dizolvat în acesta, un astfel de proces fiind denumit în mod obișnuit oxidarea metalului.
Oxidarea metalului și a impurităților sale are loc în principal datorită oxizilor de fier, agenților oxidanți solizi încărcați pe zgură, oxigenului gazos suflat în cuptor și în topitură și, într-o mică măsură, datorită oxigenului din atmosfera cuptorului. Adaosul de agenți oxidanți solizi pe zgură duce la o creștere a conținutului de oxizi de fier (Fe2O3, FeO). La interfața metal-scură, Fe2О3 este redus la FeO. În conformitate cu legea distribuției, oxigenul trece de la zgură la metal conform schemei
Oxizii de fier pot transfera la metal oxigenul din atmosfera cuptorului, inclusiv în cazul alimentării cu oxigen a spațiului de lucru, atunci când pe suprafața de contact a zgurii și a atmosferei cuptorului FeO este oxidat la Fe2O3 în conformitate cu schema
Oxidul de Fe format2O3este redus pe suprafața de contact cu metalul la FeO, ceea ce favorizează transferul de oxigen către metal datorită creșterii concentrației și activității FeO și creșterii capacității de oxidare a zgurii. Oxigenul care intră în topitură este utilizat în principal pentru oxidarea impurităților.
La suflarea oxigenului gazos direct în metalul topit, jetul de oxigen este introdus în metal, iar în această zonă, denumită diferit în literatura de specialitate (zonă de suflare, zonă de introducere, zonă de reacție), la suprafața bulelor și jeturilor are loc oxidarea directă a fierului pe schemă
Tot aici poate avea loc și oxidarea impurităților de către oxigen:
Volumul zonei de purjare este relativ mic, chiar și în convertizoarele cu oxigen nu depășește 10… 13 %. Prin urmare, oxidarea impurităților are loc în principal în restul volumului băii, numită adesea zona de circulație. Oxigenul ajunge acolo datorită dizolvării sale în fier în zona de suflare conform schemei (FeO) = Fe + [O] și transferului ulterior în volumul topiturii prin fluxuri convective.
Trebuie amintit că unele impurități din metalul topit sunt ușor oxidate de oxigen (Si, Ti, Al, V, B); unele impurități nu sunt practic oxidate (Ni, Mo, Cu, Co, W); unele impurități nu sunt complet oxidate (Mn, Cr).
Cel mai mare interes pentru metalurgiști îl prezintă reacția de oxidare a carbonului, deoarece produsul acestei reacții este monoxidul de carbon gazos CO , ale cărui bule, eliberate din topitura metalică, o agită, contribuie la egalizarea compoziției chimice a topiturii și a temperaturii acesteia, accelerează încălzirea metalului, elimină gazele dizolvate în metal, trecând printr-un strat de zgură, contribuie la spumarea acestuia.
Procesul de oxidare a carbonului în baia cuptorului siderurgic este suficient de bine studiat și poate fi descris prin următoarele scheme:
1) oxidarea de către oxigen a oxizilor de fier din zgură
2) oxidarea prin oxigen dizolvat în metal,
3) oxidarea de către oxigenul gazos sub formă de bule prinse în baie în timpul purjării cu oxigen,
O creștere a temperaturii favorizează întotdeauna o oxidare mai completă și mai rapidă a carbonului. O oxidare notabilă a carbonului se observă numai la o anumită temperatură. Supraîncălzirea minimă necesară a metalului deasupra liniei liquidus (temperatura de topire completă), la care începe procesul de oxidare a carbonului, este de 30 … 40 °C, practic este puțin mai mare.
Trebuie amintit faptul că, la oxidarea carbonului cu oxigen gazos, efectul termic total al procesului este pozitiv și se eliberează o cantitate mare de căldură; la oxidarea carbonului cu oxizi de fier din zgură, efectul termic total al procesului este negativ din cauza consumului mare de energie pentru transferul de oxigen din zgură, iar căldura este absorbită de baie. Prin urmare, oxidarea carbonului cu oxigen gazos începe, în principiu, mai devreme și poate fi utilizată, așa cum s-a menționat mai sus, pentru a accelera topirea băii. La oxidarea carbonului de către oxizii de fier din zgură, introduși în zgură de către agenții oxidanți solizi, temperatura băii poate scădea în primul rând, deoarece căldura este consumată pentru încălzirea și topirea agenților oxidanți solizi, iar apoi — la realizarea reacției de oxidare a carbonului de către oxizii de fier din zgură, viteza de oxidare a carbonului va scădea în consecință. Practic, încă de la începutul utilizării oxigenului gazos în metalurgie, chiar și în vechile ateliere cu cuptoare de mică putere s-a încercat realizarea unei oxidări combinate a carbonului cu oxidanți solizi și oxigen gazos pentru a accelera procesul.
La studierea cineticii procesului de decarburare, numeroase studii au stabilit așa-numitele concentrații critice de carbon (0,15…0,30 %), la atingerea cărora rata de oxidare a carbonului scade brusc și modul de interacțiune dintre carbon și oxigen se schimbă. În zona concentrațiilor de carbon peste concentrațiile critice de carbon, procesul de oxidare a carbonului este limitat de difuzia externă (intensitatea alimentării cu oxigen), adică prin creșterea intensității alimentării cu oxigen a topiturii, este posibilă creșterea ratei reacției de oxidare. La concentrații de carbon sub concentrațiile critice de carbon, rata de decarburare este aproape independentă de intensitatea alimentării cu oxigen și scade proporțional cu scăderea concentrației de carbon. La concentrații de carbon mai mici de 0,05%, rata de decarburare este determinată numai de difuzia carbonului la locul reacției și poate fi crescută numai prin agitarea suplimentară a topiturii.
În unele cazuri, rata procesului de decarburare poate fi determinată de procesul de eliberare a CO rezultat din oxidarea carbonului. Se știe că pentru formarea unei bule de CO în metal trebuie să se depășească presiunea coloanei de metal pм, coloana de zgură pш, atmosfera de deasupra lor patm, forța de aderență la lichid 2 σ/r, unde σ este tensiunea superficială a metalului, r este raza bulei formate:
La valori mici ale lui r valoarea 2 σ/r este uriașă și formarea bulelor de CO în volumul de metal lichid este practic imposibilă. Un astfel de proces este posibil numai la interfețele: zgură — metal; incluziune nemetalică — metal; căptușeală baie — metal; bulă de gaz — metal. Condițiile cele mai favorabile pentru formarea bulelor de CO sunt la interfața dintre căptușeală și metal, datorită rugozității căptușelii, umezelii slabe a acesteia de către metal și prezenței microporilor plini cu aer în stratul superficial al căptușelii.
Oxidarea metalului observată la sfârșitul perioadei de oxidare a topiturii este apropiată de oxidarea metalului de echilibru pentru reacția de oxidare a carbonului, dar ușor superioară acesteia (fig. 3.1). Diferența dintre concentrațiile de carbon reale și cele de echilibru este cauzată tocmai de dificultățile legate de eliberarea monoxidului de carbon (CO) în faza gazoasă.
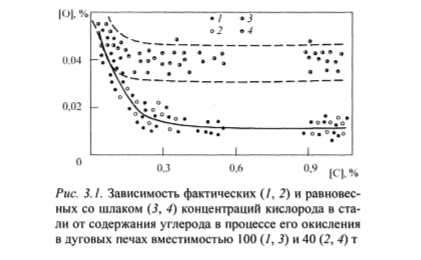
Trebuie subliniat faptul că, pentru condițiile perioadei de topire oxidativă, este destul de acceptabil să se caracterizeze oxidarea metalului prin conținutul de oxigen din metal determinat prin metoda de topire în vid. După cum se știe, această metodă permite determinarea numai a conținutului total de oxigen din metal
În timpul perioadei de oxidare a topirii, ca urmare a fierberii băii, practic toate incluziunile nemetalice care conțin oxigen sunt eliminate din baie și [O]щ = [О]dizolvare, adică tot oxigenul este dizolvat în metal. În continuare, după dezoxidarea oțelului, acesta conține anumiți produși de dezoxidare nemetalici, iar o parte din oxigen este sub formă de [O]incl. . Din cauza dificultăților de determinare a conținutului de oxigen dizolvat în metal, oxidarea metalului în astfel de cazuri este de obicei caracterizată prin valoarea activității oxigenului în metal, care este obținută prin calcul luând în considerare compoziția oțelului sau determinată prin metoda EMF direct în metalul lichid.