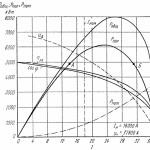
Ca și aurul, platina se găsește în minereuri și zăcăminte.
Placurile, formate ca urmare a distrugerii și transportului materialului de rocă de bază de către apele de suprafață, conțin platină sub formă de particule de aliaje cu alte metale și compuși chimici de diferite dimensiuni, de la praf fin la 30-50 mm diametru. Pepitele mai mari sunt rare, dar uneori masa lor ajunge la câteva kilograme.
Platina cu paladiu conține 7-37 % paladiu, platina cu iridiu conține până la 30 % iridiu, iar aliajele mai bogate sunt denumite pepite de iridiu.
Compușii chimici naturali includ sperrylite (PtAs2), cooperita (PtS), breggita (Pt, Pd, Ni)S și alte minerale cu o compoziție mai complexă care conțin cupru, staniu, telur, bismut și alte elemente; acestea apar separat și în agregate.
Extracția și concentrarea plachetelor sunt în multe privințe similare cu extracția și concentrarea aurului. De exemplu, materialul placentar, a cărui masă principală este platina, are următoarea compoziție:

Platina din minereurile de cupru-nichel este transformată în timpul topiturii în mată, apoi în nichel anodic și, în cele din urmă, concentrată în nămol de rafinare electrolitică. Nămolul este prelucrat pentru a extrage seleniul și telurul, crescând în același timp conținutul de metale nobile prin prăjire, levigare în acizi, topire și, în final, prin electroliză repetată: reziduul este turnat în noi anozi mici și supus dizolvării electrochimice. Ca urmare, se obțin concentrate, de exemplu, cu următoarea compoziție:
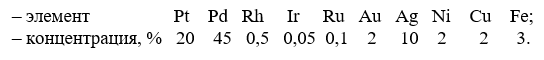
O comparație a cifrelor arată că platina este mai abundentă în schlichs și paladiul în concentrate, în timp ce aurul și argintul sunt mai frecvente în acestea din urmă. Principiile generale de bază ale prelucrării schlich-urilor și a concentratelor sunt aceleași; cu toate acestea, tehnologia din diferite uzine implică adesea etape de prelucrare diferite datorită naturii materiilor prime și condițiilor locale. Datorită proprietăților apropiate ale platinoidelor, schemele de separare a acestora sunt de obicei foarte complexe și ramificate. Omițând această diversitate, ne limităm mai jos la o scurtă descriere a uneia dintre cele mai simple variante.
Prelucrarea nămolurilor și a concentratelor
Pentru a transfera metalele nobile în soluție, a fost folosit de mult timp un amestec de acizi clorhidric și nitric — vodcă regală, cunoscut de alchimiștii antici. Acțiunea sa se explică prin oxidare și complexare simultană, după cum se poate vedea din schema următoare:
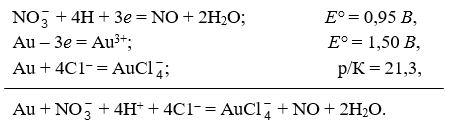
Platina, paladiul și parțial iridiul trec în soluție prin reacții similare și după următoarea schemă generală:
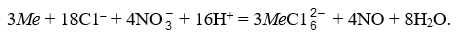
După o zi de încălzire și agitare, paladiul, aurul și platina trec aproape complet în soluție, în timp ce iridiul numai parțial. Reziduul insolubil, care are o masă de aproximativ 5 %, de exemplu, conține 30 % iridiu, 12 % ruteniu, 10 % platină și 3 % rodiu.
Platina se precipită din filtrat cu clorură de amoniu sub formă de hexacloroplatinat de amoniu (IV) dificil de dizolvat. Pentru a obține un precipitat pur, iridiul și paladiul sunt mai întâi reduse. Se utilizează diferiți agenți reducători, de exemplu sulfatul de fier (II), care precipită simultan aurul:
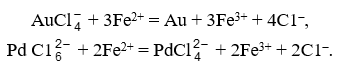
Precipitatul spălat și uscat de hexacloroplatinat de amoniu (IV) se calcinează la 800 °C, obținându-se o pulbere cenușie maleabilă de metal, buretele de platină, care necesită de obicei o purificare suplimentară complexă.
Palladium este transformat în tetracloropalladat de amoniu (II) prin adăugarea de amoniac și apoi, acidificând cu atenție soluția cu acid clorhidric, se obține un precipitat cristalin galben de trans-diclorodiaminopalladium (clorpalladozamina):
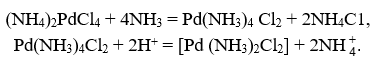
Prin calcinarea acestei săruri, se obține pulbere de paladiu.
Reziduurile de la tratarea cu vodcă tsar sunt dispersate — topite cu plumb, granulate și dizolvate în acid nitric. Argintul și plumbul intră în soluție, iar pulberea fină de platinoid pentru extracția rodiului este alipită cu bisulfat de sodiu și levigată cu apă.
Rodiul sub formă de Rh2(SO4)3 este dizolvat. Acțiunea alcalină precipită hidroxidul său, care este din nou dizolvat:
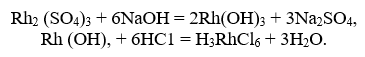
În continuare, în mediu slab acid se izolează precipitat de hexanitrorodiat de sodiu (III):
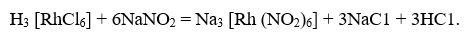
Prin acțiunea acidului clorhidric, această sare se transformă în (NH4)3RhCl6(NH RhCl), iar prin calcinare se obține buretele de rodiu.
Ruteniul și iridiul sunt sinterizate cu peroxid de sodiu la o temperatură de 500 °C. Prin levigarea sinterului se obține o soluție de Na2RuO4 și reziduu de IrO2.
Tetraoxidul de ruteniu se distilează într-un curent de clor și se absoarbe cu soluție de acid clorhidric. Adăugarea clorurii de amoniu precipită cristale brune (NH4)2RuCl6care, după uscare, sunt reduse în mediu de hidrogen pentru a obține pulbere de ruteniu la 1000 °C.
Dioxidul de iridiu este solubil în acid clorhidric. Clorura de amoniu precipită hexacloroiridat de amoniu din soluție (NH4)2IrCl6(NH IrCl), iar prin calcinarea acestuia se obține pulbere de iridiu.
Osmiul se găsește adesea sub forma unui aliaj cu iridiu — osmidă de iridiu, care nu este practic afectată de vodca tsar. Dacă este necesar să se extragă osmiul, reziduul insolubil se dispersează prin topire cu zinc și levigare cu acid clorhidric. Pulberea fină este sinterizată cu BaO2și tratată cu un amestec de acizi clorhidric și azotic, apoi osmiul este distilat sub formă de vapori de OsO foarte otrăvitori.4. În absorbantul cu soluție alcalină Na2OsO4care este redusă cu tiosulfat, iar osmiul este precipitat sub formă de sare Fremy [OsO2(NH3)4]Cl2, la calcinare se obține buretele de osmiu. Una dintre schemele de prelucrare a concentratului este prezentată în fig. 104.