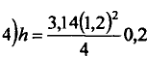Procesele observate în cuptoarele de producere a oțelului și feroaliajelor sunt caracterizate de interacțiunea fazelor metalice, de zgură și de gaz, precum și de interacțiunea componentelor din cadrul acestor faze. Să luăm în considerare interacțiunea componentelor în unele sisteme formate din substanțe gazoase și solide, faze solide și gazoase, faze lichide nemiscibile și gaze.
În cazul în care condițiile externe (temperatură și presiune) pentru un anumit sistem metalurgic rămân constante, dezvoltarea proceselor de interacțiune se desfășoară în direcția stabilirii echilibrului în cadrul acestuia. Atunci când condițiile externe se modifică, echilibrul este perturbat. În plus, o modificare a presiunii externe nu va modifica echilibrul reacției care nu este însoțită de o modificare a volumului de substanțe gazoase. Într-un sistem de echilibru format din mai multe componente, orice grup de substanțe care interacționează se află într-un echilibru similar celui care are loc în absența tuturor celorlalte componente ale sistemului.
De exemplu, într-un sistem gazos de echilibru CO-O2-CO2, caracterizat prin reacția
și constanta de echilibru K(а), starea de echilibru și constanta nu se vor modifica după introducerea în sistem a celui de-al patrulea component — carbonul, deși vor avea loc noi interacțiuni prin reacțiile
caracterizate respectiv prin constantele de echilibru K(б), К(в) și K (Г). Modificarea energiei Gibbs a reacției totale este egală cu suma algebrică a modificărilor energiilor Gibbs ale tuturor reacțiilor individuale.
De interes practic este reacția (b), pentru care
ΔG= 40800-41,70*T și lgKp = (8916/ T ) + 9,113.
Această reacție, cunoscută sub numele de reacție Bem-Boudoir, își are originea în reducerea oxizilor metalici cu carbon. Boudoir a studiat experimental echilibrul în sistemul oxigen-carbon.
În practică, procesele de reducere prin reactivi carbonici se realizează în majoritatea cazurilor prin intermediul fazei gazoase. De exemplu, reducerea prin reacția FeOтв + CO ⇔ Fe + C02 asigură un contact bun al gazului cu suprafața FeO solid.
Reducerea siliciului din silice se realizează prin contactul bucăților de cocs și cuarț și interacțiunea cu oxidul de carbon prin reacțiile
SiO 2 + 2C⇔ Si + 2CO,
SiO2 + 2CO ⇔ Si + 2C02,
Participarea fazei gazoase la reducerea siliciului asigură continuitatea procesului până la epuizarea completă a oricăruia dintre componente. Reducerea oxizilor metalici prin monoxid de carbon este descrisă în general prin reacția MeO + CO ⇔ Me + C02. Constanta de echilibru a acestei reacții de reducere indirectă Kr = pCO2/ рCO, adică este egală cu raportul dintre presiunile parțiale ale gazului carbon și ale oxidului de carbon.