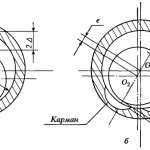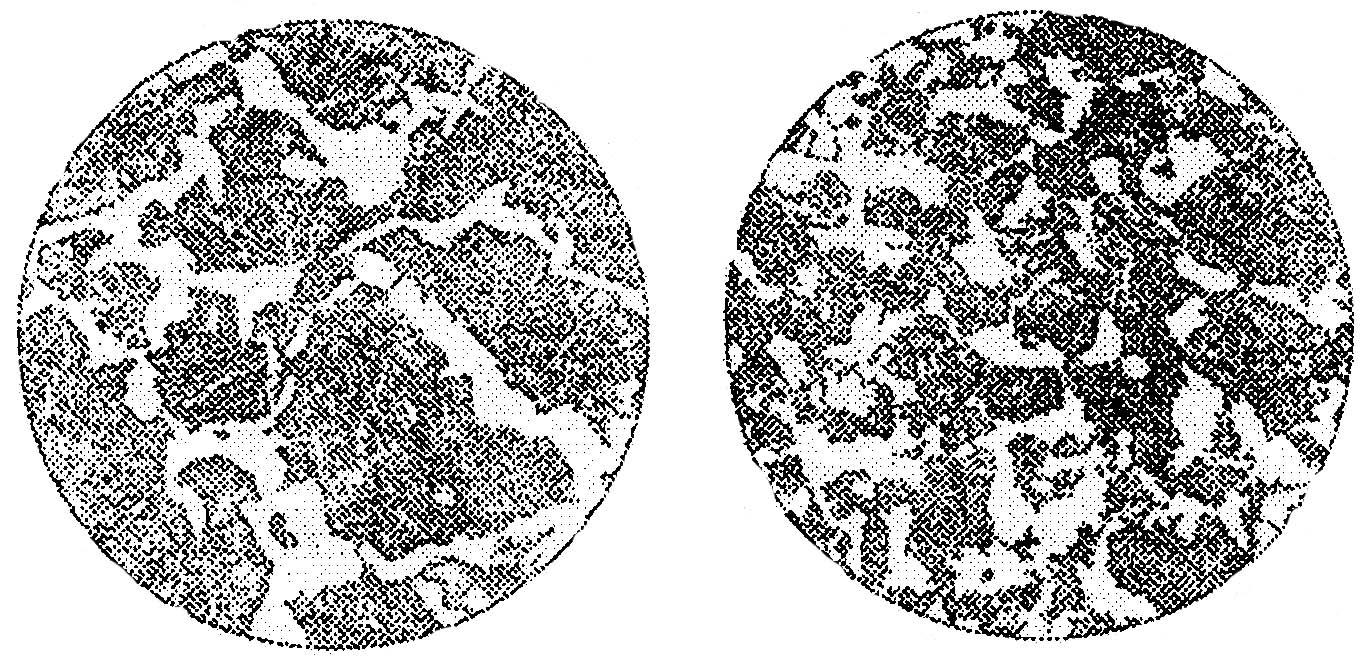
Toate metalele sunt caracterizate de o structură unică: au o distribuție perfect organizată a atomilor. Aceasta explică principalele lor proprietăți. Legătura seturilor de atomi formează o rețea cristalină, alcătuită din cristale elementare. Dar atunci când metalele sunt expuse la temperatură, structura lor se modifică. Aceasta se numește cristalizare a metalelor.
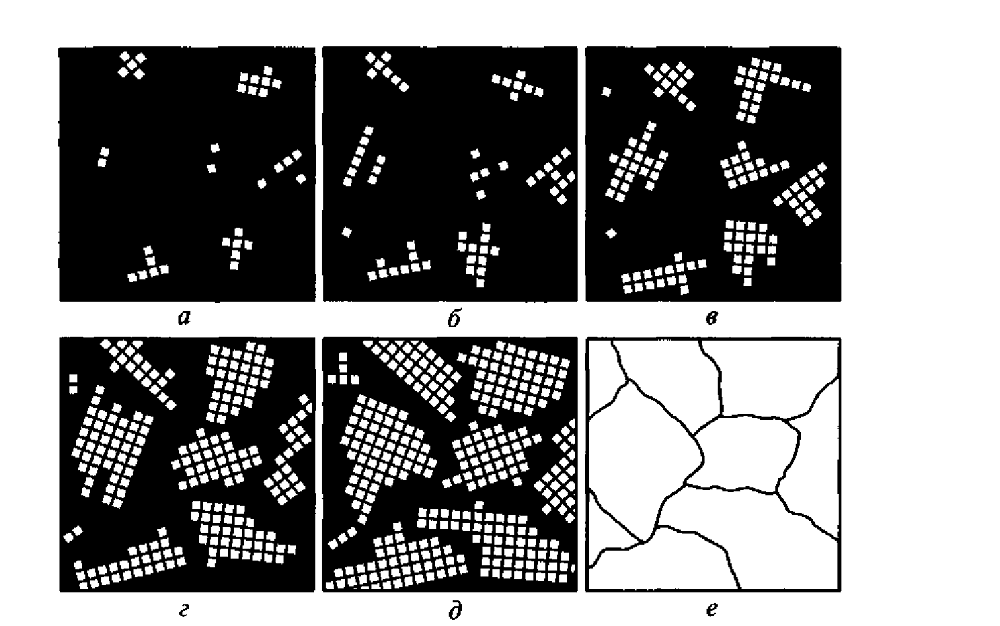
Cristalizarea este definită ca procesul de transformare a unei substanțe chimice dintr-o soluție lichidă într-o stare cristalină solidă prin schimbarea temperaturii și a fazelor. Aceasta are loc în natură, dar este cel mai adesea realizată chimic în laborator. În 1878, studiind structura oțelului lichid, din care sunt fabricate butucii și alte elemente, oamenii de știință au demonstrat că cristalizarea constă în două procese. Primul constă în formarea de particule mici, care sunt numite „nuclee” sau centre, iar al doilea — în creșterea cristalelor din aceste centre.

Caracteristici ale procesului de cristalizare a metalelor
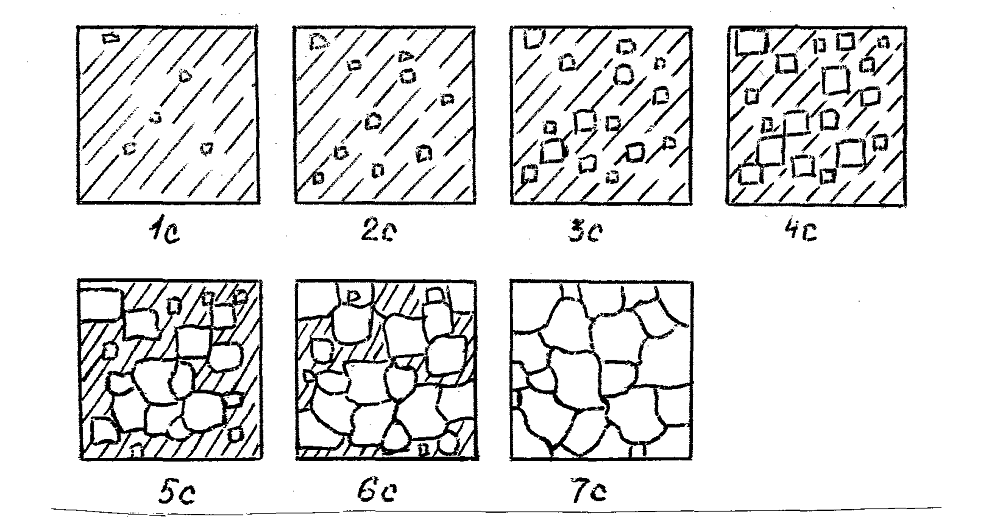
Cristalizarea metalelor și a aliajelor se bazează pe principiile solubilității: în general, compușii sunt mai solubili în lichide calde (solvenți) decât în cele reci. Prin înțelegerea procesului în sine și selectarea parametrilor corecți, este posibil să se producă în mod repetat cristale de dimensiunea, forma și puritatea necesare, reducând la minimum problemele de prelucrare din aval.
Etapele de bază ale acestui proces sunt următoarele:
- Se selectează un solvent. Este important să se ia în considerare cantitatea exactă de substanță care urmează să fie dizolvată.
- Produsul este dizolvat în solvent, iar temperatura este crescută până când toate substanțele solide sunt dizolvate.
- Următorul pas în procesul de cristalizare a metalelor implică reducerea solubilității prin suprarăcire, evaporare sau altă reacție.
- Efectuarea cristalizării propriu-zise. Pe măsură ce solubilitatea scade, se ajunge la un punct în care cristalele se nuclează și apoi cresc. În cele din urmă, ar trebui să se formeze cristale de produs de înaltă puritate, iar impuritățile ar trebui să rămână în soluție.
- În continuare, trebuie atins echilibrul de temperatură pentru a maximiza randamentul produsului solid.
- Etapa finală este filtrarea și uscarea produsului purificat.
Cristalizarea metalelor este o metodă utilizată de mult timp pentru purificarea materiei. Este destul de complexă, deoarece această precipitare trebuie să fie lentă pentru a obține o puritate ridicată a solidului cristalizat. Dacă substanța se solidifică prea repede, impuritățile pot rămâne în ea.
După cum a devenit deja clar, formarea cristalelor are loc prin solidificare. În cazul metalelor pure, aceasta are loc la temperaturi constante, în timp ce în aliaje se modifică în timpul procesului de solidificare. Aceasta este principala diferență dintre cristalizarea metalelor pure și a aliajelor.
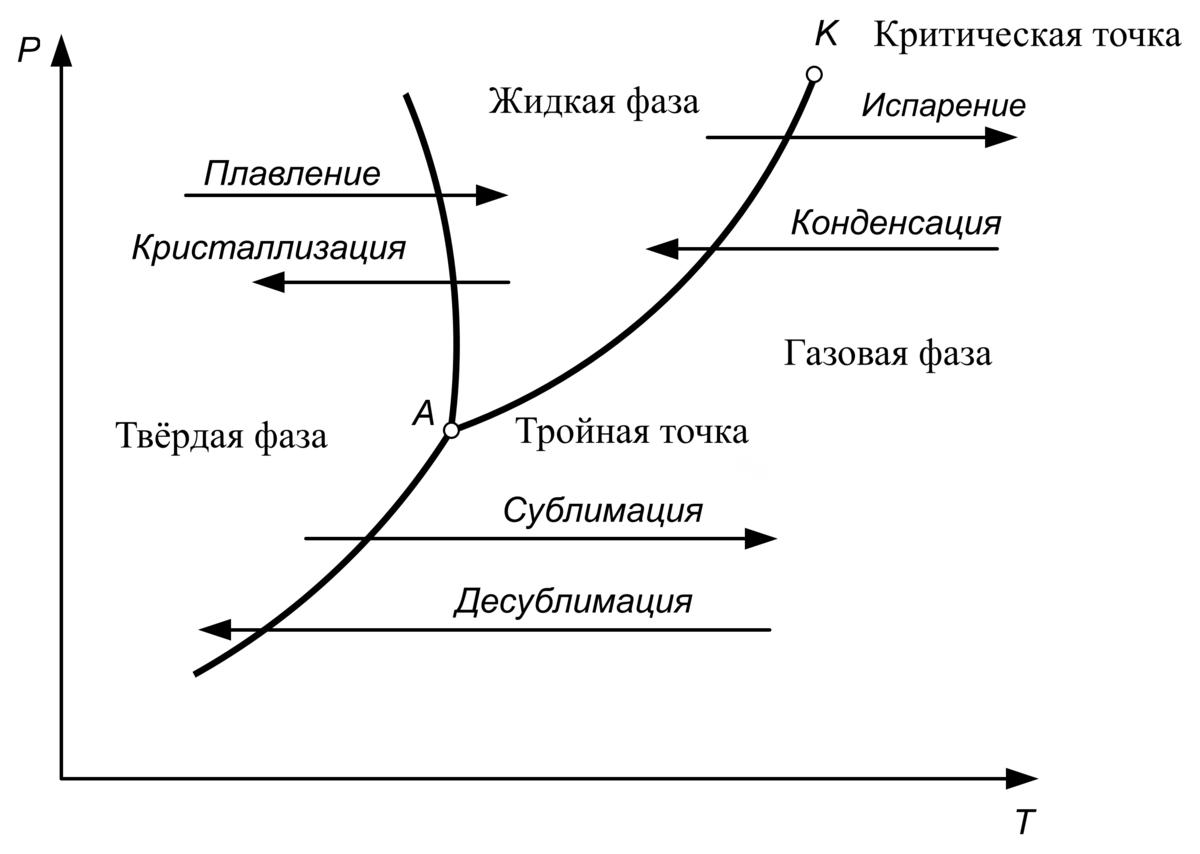
Metode de cristalizare
Procesul de cristalizare a unui metal sau a unui aliaj este o tehnologie populară utilizată în diferite sfere de activitate. Există mai multe metode diferite cunoscute astăzi:
- evaporarea solventului: este necesară o cantitate mare de material, dar opțiunea este considerată simplă și eficientă;
- răcire lentă: utilizează un solvent cu un punct de fierbere mai mic de 100°C;
- difuzia solventului sau a vaporilor — funcționează bine cu cantități mici de material, dar este dificil de găsit un solvent adecvat;
- sublimarea — se face la temperaturi ridicate, ceea ce face ca cristalele să crească prea repede și este dificil de controlat.
Alegerea celui mai adecvat depinde în principal de proprietățile materialului care cristalizează. Ați avut acum o scurtă introducere în cristalizarea metalelor, învățând despre condițiile de bază, temperatură și modul exact în care aceasta se desfășoară.